Merck pide autorización para su píldora contra el coronavirus
Molnupiravir podría ser el primer medicamento antiviral oral para el tratamiento de COVID-19. Fue aprobado en 170 países, entre ellos Argentina. Según los primeros estudios, redujo un 50 por ciento "el riesgo de hospitalización o muerte".

El logotipo de la compañía Merck & Co. en su sede de Rahway, Estados Unidos. Foto: EFE | Justin Lane.
El empresa farmacéutica Merck informó que solicitó a las autoridades sanitarias de los Estados Unidos la autorización para el uso de emergencia de su medicamento Molnupiravir, una píldora experimental contra el coronavirus para pacientes graves.
En un comunicado difundido este lunes, Merck anunció el pedido a la Administración de Medicamentos y Alimentos (FDA por sus siglas en inglés) para el Molnupiravir, en asociación con Ridgeback Biotherapeutics.
La empresa señaló que “si se autoriza, Molnupiravir podría ser el primer medicamento antiviral oral para el tratamiento de COVID-19”.
Se trata de “un medicamento antiviral oral en fase de investigación para el tratamiento del Covid-19 de leve a moderado en adultos que corren el riesgo de evolucionar a Covid-19 grave y/o de ser hospitalizados”.
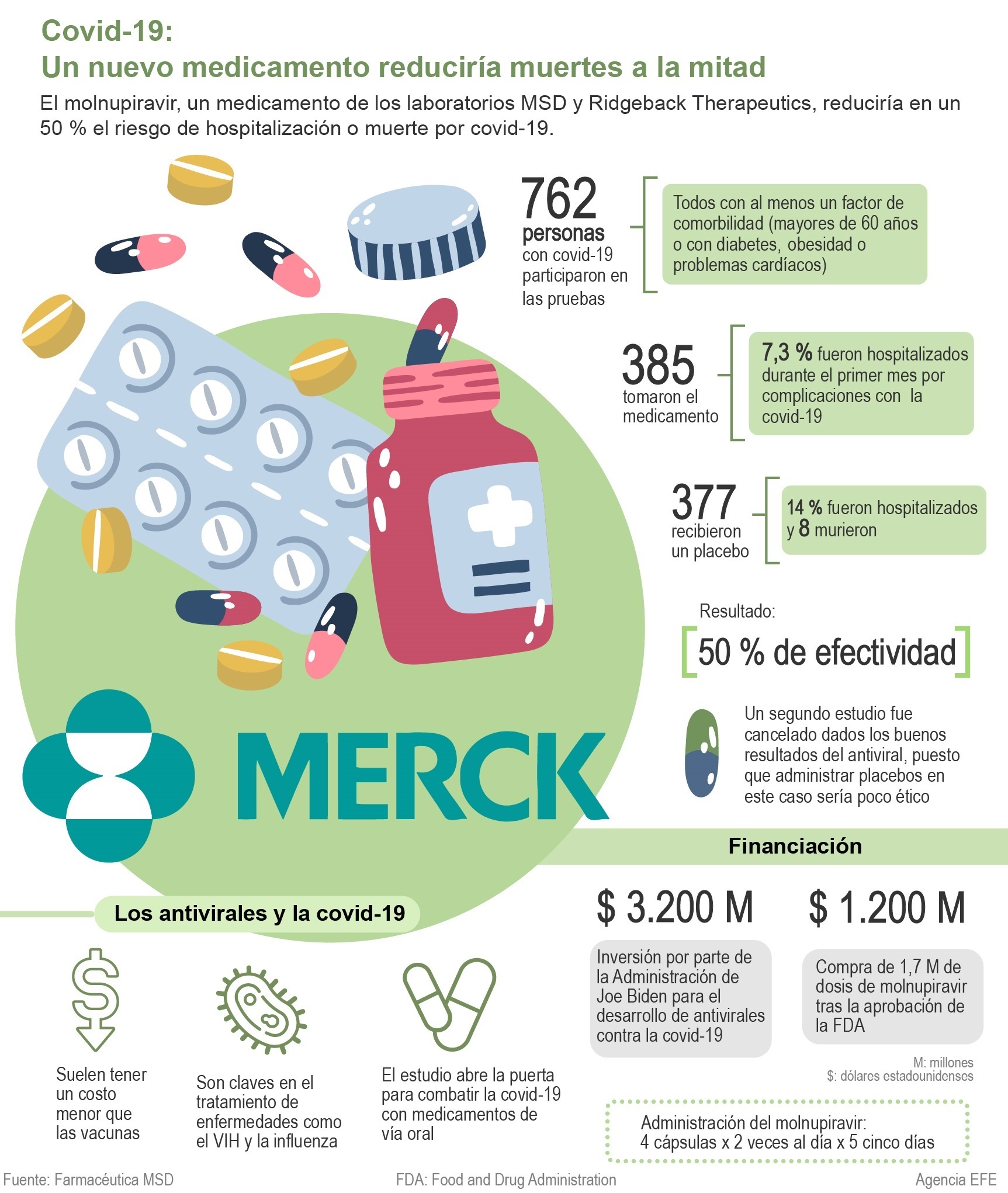
El medicamento había sido presentado el pasado 1 de octubre y entonces, el laboratorio aseguró que el Molnupiravir “redujo el riesgo de hospitalización o muerte en aproximadamente un 50 por ciento en comparación con el placebo para pacientes con COVID-19 leve o moderado en el análisis intermedio positivo del estudio de fase 3”.
El medicamento fue probado en 170 países, entre ellos la Argentina.
Ahora Merck espera que la aprobación de la FDA para poder venderlo, mientras aguarda también que otras agencias reguladoras también autoricen su uso.
El anuncio se produjo el mismo día en que el laboratorio británico-sueco AstraZeneca anunció que un cóctel de anticuerpos contra el coronavirus dio resultados positivos en los ensayos clínicos de fase 3.
De esta manera, se abre un nuevo camino para el tratamiento del coronavirus que va más allá de las vacunas y tiene como objetivo a las personas que ya contrajeron el virus.

